PROČ PATŘÍ ENTYVIO® DO PŘEDNÍCH LINIÍ?
Protože jde o dlouhodobé cíle – při dosažení endoskopické a histologické remise můžeme změnit vývoj onemocnění. Protože může dosáhnout i transmurálního zhojení.1
Protože má všeobecně známý příznivý bezpečnostní profil a je to jediné GIT selektivní biologikum.2,3
Protože má velmi nízkou imunogenicitu; pacienti mají dlouhou perzistenci na léčbě.5
Protože pravděpodobně neovlivní další linie léčby.5
Protože máte možnost volby – subkutánní i intravenózní formy.3
- Krátkodobé cíle = kontrola symptomů6
Dlouhodobé cíle = hluboká remise (endoskopická remise, histologická remise, transmurální zhojení)6
Modifikace onemocnění!7
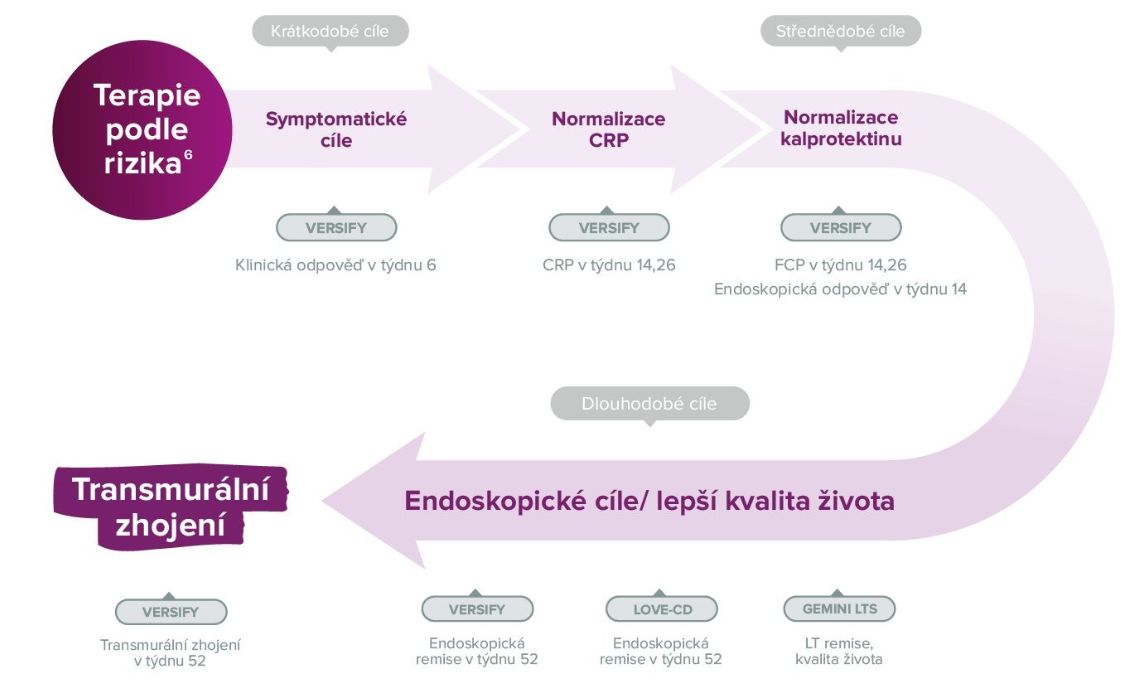
PRŮKAZ HLOUBKY ÚČINNOSTI LÉKU ENTYVIO®
anti-TNF naivní pacienti, vše hodnoceno v týdnu 52
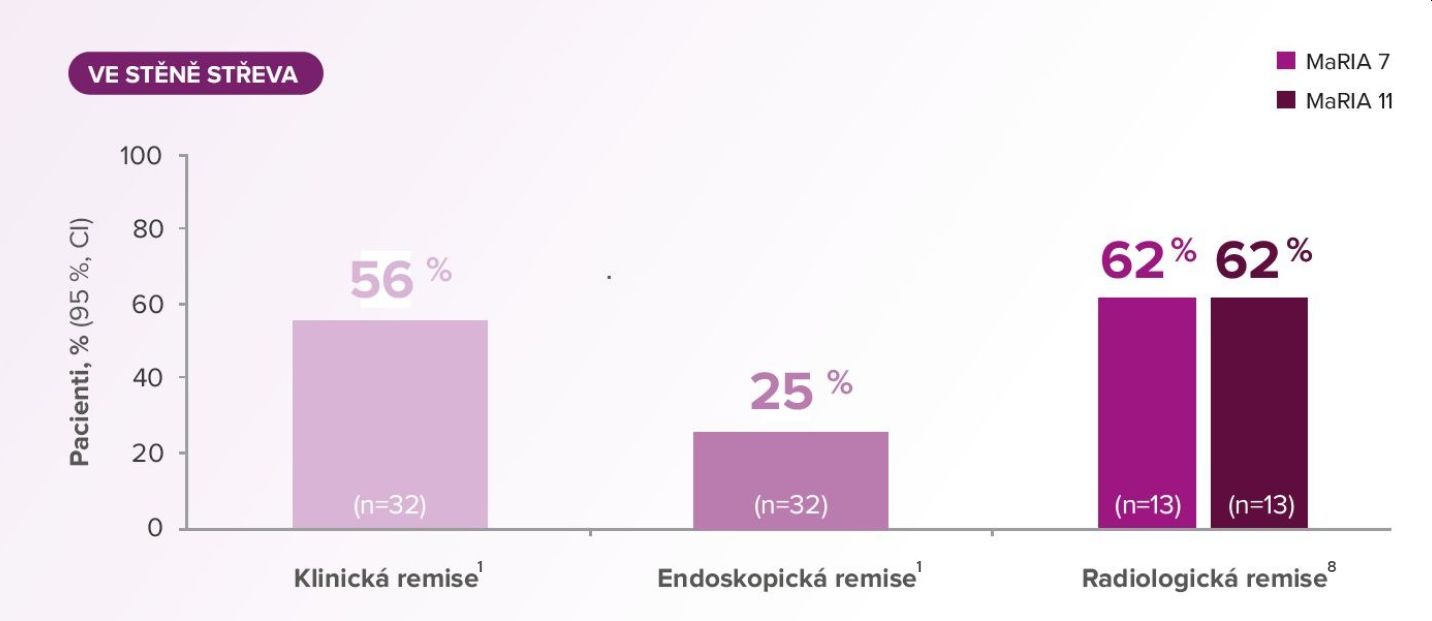
Post hoc analýza studie Versify, pomocí MRE (Magnetic Resonance Enterography).
MaRIA skóre – Magnetic Resonance Index of Activity Score MaRIA – 7 ukazuje remisi všech aktivních lézí (skóre <7ve všech segmentech střeva) a MaRIA – 11 ukazuje zlepšení pouze těžkých lézí (skóre<11ve všech segmentech střeva). Radiologická remise - MaRIA < 7 ve všech segm. střeva u pac., kteří na počátku měli MaRIA skóre ≥ 7 v alespoň 1 střev. segm.
PRŮKAZ HLOUBKY ÚČINNOSTI LÉKU ENTYVIO®
anti-TNF naivní pacienti, vše hodnoceno v týdnu 52
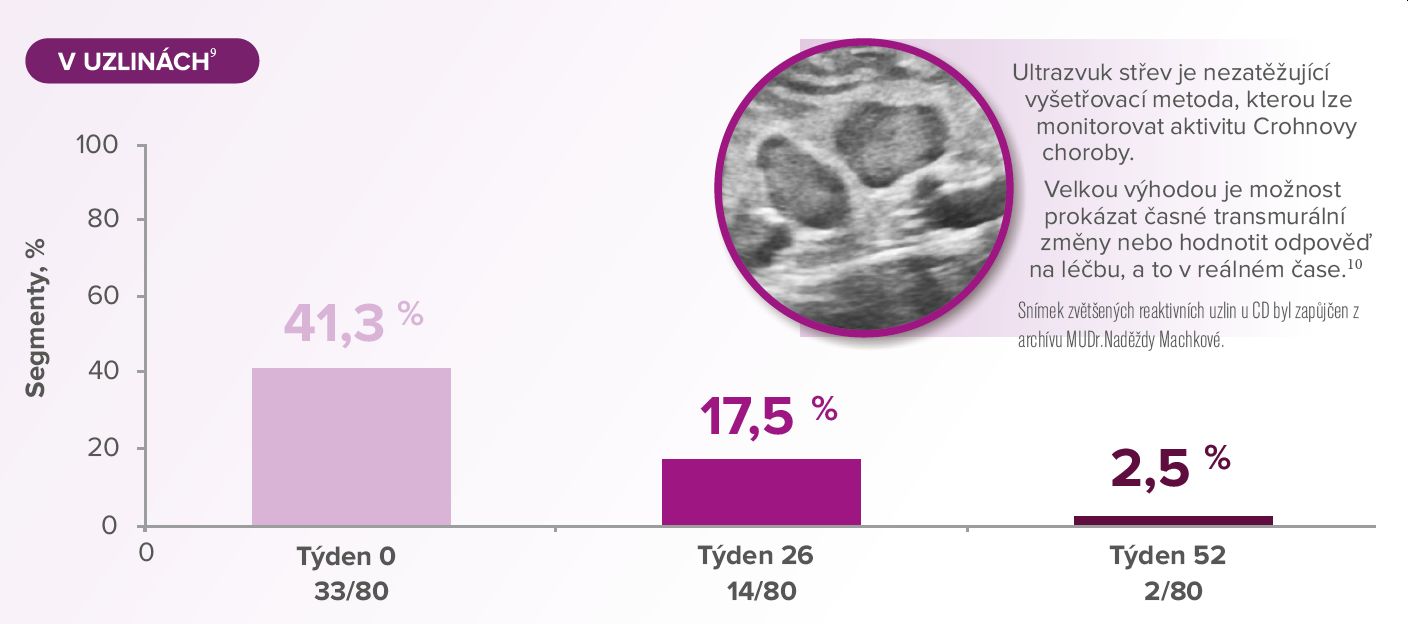
Post hoc analýza studie Versify, pomocí MRE (Magnetic Resonance Enterography)
Lymf. uzliny byly kvantif. v segmentech: rektum, sigma, c. ascendens, c. transversum a c. descendens (vč.TI, hodnoceno jako 1 segment), hodnotily se v týdnu 0, 26 a 52. Všechny segmenty měly skóre
MaRIA ≥7; a v týdnu 0 více jak 5 zvětšených lymfatických uzlin.
VERSIFY1 : prosp., multicentr. studie pac. se stř. těžkou až těžkou akt. CD, rozdělenou na část A (26 týdnů) a část B (26 týdenní rozšíření). Open-label forma: VDZ 300 mg i.v. v týdnech 0, 2 ,6 a potom každých 8 týdnů, bez možnosti dávky v týdnu 10. Prim. cíl: endoskop. remise (SES-CD ≤ 4) v týdnu 26. Sek. cíl: kompletní slizniční zhojení (absence ulcerací, včetně aft) v týdnu 26 a 52; Exploratorní cíl: změny v transmurální aktivitě použitím MRE (MaRIA) v týdnu 26 a 52. MaRIA-7 remise všech aktivních lézí (skóre <7 ve všech střevních segmentech).
LOVE CD11: prosp., multicentr. open – label studie u pac. se stř. těžkou až těžkou akt. CD (počet pac. 110). VDZ 300 mg i.v. týden 0, 2, 6 a potom každých 8t, s možnou dávkou v 10t. Prim. cíl: CDAI (CD act. Index) remise =
CDAI < 150 a současně bez léčby kortikoidy. Jedná se o kombinovaný endpoint. V registračním programu Gemini II dosaženo klinické remise u 39 % pacientů z celkového počtu 154 v 52. týdnu.
GEMINI LTS12 : prosp., multicentr. open – label studie u pac. se stř. těžkou až těžkou akt. UC a CD z programu Gemini a pac. s nově nasazeným VDZ. Počet pac. UC = 894; CD = 1349, VDZ 300 mg i.v. každé 4t. Primárním cílem bylo
hodnocení dlouhodobé bezpečnosti.
Reference:
1. Danese et al., Gastroenterology 2019, 157:1007-1018 2. Colombel J-F et al. Gastroenterology 2017;152:351–361. 3. SPC Entyvio 03/2025 4. Singh et al., Aliment Pharmacol Ther. 2019;50:848–857 5. Bressler B, et al., Journal of Crohn´s and Colitis, 2021, 1-13. 6. Turner D. et al. Gastroenterology 2021;160:1570–1583. 7. Peyrin-Biroulet L, et al. Clin Gastroenterol Hepatol. 2014;12:929–34. 8. Rimola J et al. United European Gastroenterol J 2018; 6(Suppl 1):A68, Abstr OP175. 9. Rimola J, et al. Clin Exp Gastroenterol. 2024 Jan 27;17:9-23 10. Kucharzik T, Wittig BM, Helwig U, et al. Use of intestinal ultrasound to monitor crohn's disease activity. Clin Gastroenterol Hepatol 2017;15:535–542.e2.11. Löwenberg M., et al. Gastroenterology 2019; 157: 997-1006. 12. Loftus EV Jr, et al. Aliment Pharmacol Ther. 2020;52:1353-65.
C-APROM/CZ/ENTCD/0077
Datum přípravy: 08/2025

